Азотты қышқыл


Азотты қышқыл HNO2 - сұйық ертінді түрінде ғана кездесетін бір негізді, әлсіз қышқыл.
Түсі - ақшыл аспан көк.
Тұздары - нитриттер - улы, күшті электролиттер, түгелдей дерлік суда жақсы ериді. Ең маңыздысы - натрий нитриты, медицинада қолданады.
Молекула құрылымы
Газтәріздес сәтінде азотты қышқылдың молекуласы 2 конфигурацияда болады:
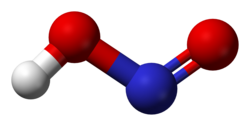 |
 |
Екінші құрылымы тұрақты болып келеді, себебі цис-HNO2(г) DG°f = −42,59 кДж/моль, ал транс-HNO2(г) DG = −44,65 кДж/моль.
Химиялық қасиеттері
Сулы ертіділерде тепе-теңдік сақталады:
Қыздырғада азот оксиді(ІІ) NO мен азот қышқылы құралады:
Азотты қышқыш - әлсіз, сулы ертіділерді диссоциация жасайды. Сірке қышқылынан күштірек. Тұздардан қүшті қышқылдармен ығыстырылады:
Тотықтырғыш та тотықсыздандырғыш та қасиет көрсете алады. Күшті тотықтырғыштар (КMnO4, К2 Сr2O7, H2O2 т.б.) оны азот қышқылына дейін тотықтырады:
Күшті тотықсыздандырғыштар (KJ, H2S т.б.) азот тотығына дейін тотықсыздандырады:
Азотты қышқыл мен оны тұздарының ертіндісіне KJ және крахмал ертінділері құйса, ертідінің түсі көгереді.
Алынуы
Азотты қышқылды суға азот оксидін(ІІІ) еріткенде алуға болады:
Және азот оқсиді(IV) суға еріткенде алынады:
Дереккөздер
- “Қазақстан”: Ұлттық энциклопедия/Бас редактор Ә. Нысанбаев – Алматы “Қазақ энциклопедиясы” Бас редакциясы, 1998